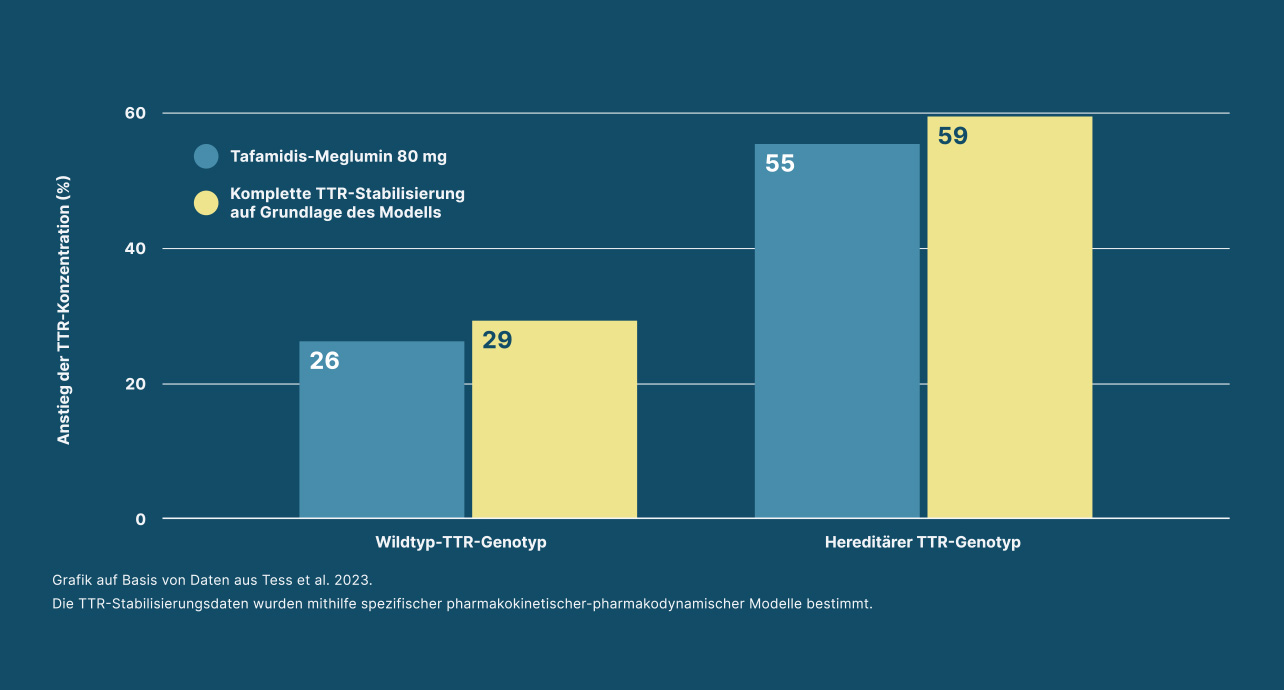
TTR = Transthyretin.
* Vyndaqel® (Tafamidis) 61 mg und Vyndaqel® (Tafamidis-Meglumin) 80 mg sind indiziert zur Behandlung der Wildtyp- oder hereditären Transthyretin-Amyloidose bei erwachsenen Patient:innen mit Kardiomyopathie.9 Eine einzelne Kapsel Vyndaqel® 61 mg ist bioäquivalent zu Vyndaqel® 80 mg (vier Kapseln zu 20 mg). Diese sind auf Basis der mg-Angabe nicht gegeneinander austauschbar.14
† Eine nahezu vollständige Stabilisierung entspricht einer Verringerung der TTR-Dissoziationsrate, gemessen mit dem Subunit Exchange Assay, um >90 %. Die Untersuchung wurde in vitro in menschlichem Plasma durchgeführt.10
- Colon W, Kelly JW. Biochemistry. 1992; 31(36):8654–8660.
- Lai Z, Colon W, Kelly JW. Biochemistry. 1996;35(20):6470–6482.
- Hammarstrom P et al. Science. 2003;299(5607):713–716.
- Hammarstrom P, et al. Science. 2001;293(5539):2459–2462.
- Rappley I et al. Biochemistry. 2014;53(12):1993–2006.
- Magalhães J, et al. Cell Mol Life Sci 2021;78(17-18):6105–6117.
- Liz MA, et al. Neurol Ther 2020;9(2):395–402.
- Damy T et al. Eur J Heart Fail. 2021;23(2):277–285.
- Fachinformation Vyndaqel® 61 mg, aktueller Stand.
- Tess DA et al. Amyloid. 2023;30(2):208–219.
- Hund E et al. Aktuelle Neurologie. 2018;454:605–516.
- Bulawa CE et al. Proc Natl Acad Sci. 2012;109:9629–9634.
- Maurer MS et al. Circ Heart Fail. 2017;10:e003815.
- Lockwood PA et al. Clin Pharmacol Drug Dev. 2020;9(7):849–854.